Nuestros patronos Miguel Carasol y Javier Román, junto al Prof. Mariano Sanz, revisan los conocimientos actuales sobre el tema: “ASOCIACIÓN ENTRE PERIODONTITIS Y DIFERENTES TIPOS DE CÁNCER”. Se debe resaltar que el artículo incluye recomendaciones sencillas sobre higiene, prevención y tratamiento de complicaciones antes, durante y después de los tratamientos oncológicos.
(Artículo Publicado en la revista Perio Cínica (Nº 32) de SEPA)

Mariano Sanz. Catedrático de la Sección de Periodoncia, Departamento de Especialidades Clínicas Odontológicas, Facultad de Odontología, Universidad
Complutense de Madrid. Director del Grupo de Investigación ETEP (Etiología y Terapéutica de las Enfermedades Periodontales y Periimplantarias), Universidad Complutense de Madrid.
Javier Román. Cofundador y director médico asistencial del IOB Institute of Oncology, Madrid. Profesor coordinador de Oncología, Universidad Europea de Madrid. Patrono y presidente de la Fundación Oncoayuda.
Miguel Carasol. Grupo de Investigación ETEP (Etiología y Terapéutica de las Enfermedades Periodontales y Periimplantarias), Universidad Complutense de Madrid. Coordinador de Alianza por la Salud Periodontal y General, Sociedad Española de Periodoncia (SEPA).
RESUMEN
EL CÁNCER y la periodontitis son dos grupos de enfermedades muy prevalentes, aunque evidentemente con una morbimortalidad muy diferente. Conforme se conoce más sobre la etiología y los factores de riesgo para el cáncer, dada la condición de la periodontitis como una enfermedad infecciosa crónica que genera un proceso inflamatorio de bajo grado, se podría incluir en el grupo de factores de riesgo para ciertos tipos de tumores, sobre todo de los que más evidencia científica existe, como el cáncer orofaríngeo, tumores malignos del tracto digestivo superior y cáncer de páncreas.
Los objetivos de la presente revisión son (1) analizar la situación del cáncer en España;
(2) abordar los mecanismos propuestos para la asociación entre periodontitis y cáncer y describir la evidencia epidemiológica a partir de estudios transversales y longitudinales; (3) describir qué tipos de tumores podrían asociarse en grado diferente con la periodontitis; y, finalmente, (4) dada la prevalencia de ambas enfermedades, se aborda el manejo del paciente oncológico en la consulta dental, tanto antes como durante o después de las diferentes terapias que reciben los pacientes en función del tipo de tumor, estadio del mismo y fase terapéutica en la que se encuentran. De esta manera, se pretende prevenir o mitigar las complicaciones que pueden presentarse en la consulta dental, incidiendo sobre todo en la necesaria relación entre los oncólogos y el equipo odontológico.
SITUACIÓN GENERAL DEL CÁNCER EN NUESTRO ENTORNO
EL CÁNCER ES UNA DE LAS PRINCIPALES CAUSAS de mayor morbimortalidad a nivel global. Los datos para España presentados en esta sección se han extraído del informe
publicado por SEOM (Sociedad Española de Oncología Médica) en 2025 (Figura 1) (REDECAN 2025). Es importante tener en cuenta esta información por la relevancia que tiene el paciente oncológico para la consulta dental y, a su vez, por el efecto de la patología periodontal sobre la prevención, tratamiento y complicaciones del cáncer en sus diferentes fases.

Figura 1. Las cifras del cáncer en España, 2025 según la Sociedad Española de Oncología Médica.
Incidencia del cáncer
En España se prevén para 2025 unos 296 103 casos nuevos de cáncer, de los cuales 166 513 corresponden a hombres y 129 590 a mujeres. A nivel de la cavidad oral y faringe, se estiman 7446 casos nuevos de cáncer, de los cuales 5221 corresponden a hombres y 2235 a mujeres.
En el futuro se espera un incremento de la incidencia de cáncer, alcanzando los 350.000 casos nuevos en España en 2050 (Cancer Incidence 2025).
Prevalencia del cáncer
La prevalencia total es el número de casos de cáncer de todos los pacientes que habiendo sido diagnosticados siguen con vida en un momento concreto. En España es de 2 265 152 casos, de los que 1 066 959 corresponden a hombres y 1 198 193 a mujeres.
A nivel de la cavidad oral y faringe la prevalencia se estima en 58 353 casos, 40 087 en hombres y 18 266 en mujeres (Verdecchia y cols. 2002).
Mortalidad debida al cáncer
El cáncer es la segunda causa de mortalidad global después de las enfermedades cardiovasculares, pero es la primera causa de mortalidad en varones. La mortalidad total anual en España por todas las causas se estima en 436 124 personas, siendo de 115 429 por cáncer, 68 164 hombres y 47 267 mujeres. Los tumores de cavidad oral y faringe serán responsables de 2469 muertes, 1742 hombres y 727 mujeres (INE 2023).
Supervivencia a 5 años por cáncer
Globalmente, el 55,3 % en los hombres y el 61,7 % en las mujeres sobreviven al cáncer a los 5 años. En cuanto a los tumores de cavidad oral y faringe, sobreviven el 38,2 % de los hombres y el 57,2 % de las mujeres (De Angelis y cols. 2014).
¿Con qué tipos de cáncer sería más frecuente atender a pacientes en una consulta dental? Pacientes con tumores “en fase activa”
Los cánceres más frecuentes en hombres serán los de próstata (32 188), pulmón (23 442), vejiga urinaria (18 281), colon (18 312) y recto (8912).
En las mujeres serán los de mama (37 682), colon (11 999), pulmón (11 064), cuerpo uterino (7428) y recto (5350).
Pacientes con tumores “en fase inactiva”
En España hay más de 2 265 000 personas que han tenido algún tipo de cáncer y siguen viviendo, de los que más de 500 000 son cánceres de mama. Por detrás está el cáncer colorrectal con 340 089 casos en ambos sexos, y en tercer lugar hay 259 788 varones vivos con cáncer de próstata (REDECAN 2025).
Situación actual del tratamiento del cáncer
Los tratamientos más complejos como la quimioterapia de altas dosis con trasplante autólogo o heterólogo de médula ósea; los tratamientos que incluyen radiación de la cabeza y cuello con quimioterapia e inhibidores de EGFR (receptor del factor de crecimiento epidérmico) o inmunoterapia; los fármacos antieméticos; los inhibidores de tirosina-quinasa; la inmunoterapia; los antiangiogénicos; los antirresortivos óseos; los inmunoconjugados y las terapias CAR-T son las nuevas armas que los oncólogos administran para el control de la enfermedad.
Factores de riesgo para el cáncer
Los factores de riesgo evitables del cáncer son tanto los derivados de la conducta de las personas como los ambientales y metabólicos, siendo los primeros los más numerosos y estando el tabaquismo a la cabeza de todos, responsable de hasta un 33 % de cánceres a nivel mundial y de hasta el 22 % de las muertes por cáncer. El 47 % de los cánceres podrían evitarse si desapareciesen estos factores y hasta un tercio si se desterrase el tabaquismo, el consumo de alcohol y la obesidad. Se han definido 10 factores de riesgo oncológico que son la causa de casi la mitad de los casos de cáncer (GBD 2019 Cancer Risk Factors Collaborators 2022), varios de los cuales son también factores de riesgo para las periodontitis (Genco y cols. 2013). Por orden de importancia son:
1. Tabaquismo.
2. Alcohol.
3. Obesidad.
4. Sexo inseguro.
5. Diabetes.
6. Polución ambiental.
7. Asbestosis profesional.
8. Dieta pobre en cereales.
9. Dieta pobre en leche.
10. Humo de tabaco de 2.ª mano.
ENFERMEDADES PERIODONTALES Y CÁNCER: ESTUDIOS EPIDEMIOLÓGICOS Y POSIBLES MECANISMOS
Introducción
Como se ha comentado previamente, el cáncer es la segunda causa de muerte en el mundo. Aunque el cáncer se considera una enfermedad genética producida por un acúmulo de mutaciones en los mecanismos de división de distintas poblaciones celulares y, por lo tanto, el enfermo de cáncer presenta un riesgo intrínseco no modificable, se estima que en más del 30 % de los procesos malignos se pueden asociar factores de riesgo modificables, fundamentalmente el abuso del tabaco, del alcohol, presentar un índice de masa corporal alto o sufrir de infecciones crónicas. En los últimos años se ha estudiado el posible papel del microbioma como mecanismo puente entre los factores sistémicos carcinogénicos y los procesos inflamatorios crónicos locales en la iniciación y progresión de las neoplasias (Plummer y cols. 2012).
La periodontitis es una enfermedad inflamatoria crónica con una prevalencia muy elevada, siendo en España del 38 % de los adultos en el rango de 35 a 44 años y de más del 60 % entre las personas mayores de 55 años (Carasol y cols. 2016), y que se manifiesta con destrucción de los tejidos de soporte dentario a nivel local, pero que ocasiona una inflamación sistémica de bajo grado de intensidad y una translocación bacteriana por vía plasmática. De hecho, estos mecanismos han servido como plausibilidad biológica que explica las múltiples asociaciones epidemiológicas entre la periodontitis y las enfermedades no transmisibles más frecuentes (p. ej., diabetes y enfermedades cardiovasculares). Igualmente, estudios epidemiológicos han asociado un mayor riesgo de cáncer en pacientes con periodontitis o que han perdido sus dientes por causas periodontales (Baima y cols. 2024). Por lo tanto, el estudio de estas asociaciones epidemiológicas y de los mecanismos que pueden explicarlas representa una nueva vía de investigación en el estudio de la posible fisiopatología oncogénica de las infecciones crónicas locales, en este caso utilizando el modelo de la periodontitis. En esta revisión se actualizará el conocimiento de las asociaciones epidemiológicas, tanto de cánceres locorregionales como de procesos oncológicos a distancia. Igualmente, se tratará de desentrañar los mecanismos que puedan explicar dichas asociaciones para, de este modo, calibrar su impacto en la salud pública y en el desarrollo de futuras estrategias preventivas.
Asociación epidemiológica Periodontitis y riesgo total de cáncer
Existen pocos estudios epidemiológicos que hayan estudiado la asociación entre periodontitis e incidencia de cáncer total. Michaud y cols. (2008) realizaron una revisión sistemática con metaanálisis de estudios que han valorado la asociación epidemiológica entre periodontitis, pérdida de dientes y riesgo de cáncer. Un total de 18 estudios (13 de cohortes y 5 de casos y controles) han valorado la asociación entre periodontitis y riesgo de cáncer, mientras que 34 (14 de cohortes y 20 de casos y controles) han estudiado la asociación entre pérdida de dientes y riesgo de cáncer. En general, y aunque existe gran variabilidad en el modo de evaluar la exposición (periodontitis), se ha observado una asociación positiva de esta enfermedad con el riesgo total de cáncer en 5 estudios de cohortes. Igualmente, se han reportado asociaciones significativas entre periodontitis y cáncer bucal, de pulmón y de páncreas.
El primer trabajo que examinó la relación entre periodontitis y la mortalidad por cáncer fue el Estudio de Seguimiento Epidemiológico de la Encuesta Nacional de Examen de Salud y Nutrición (NHANES) I, que estudia la población adulta de EE. UU. La mortalidad por cáncer se asoció positivamente con la periodontitis (HR IC 95 %: 1,55; 1,25-1,92), especialmente para la mortalidad por cáncer de pulmón (HR IC 95 %: 1,94; 1,16-3,26). Cuando se estratificó por tabaquismo, la periodontitis se asoció con cáncer de pulmón en fumadores (HR IC 95 %: 1,94; 1,14-3,30), pero no en los nunca fumadores (HR IC 95 %: 0,58; 0,12-2,78) (Hujoel y cols. 2003).
En un estudio prospectivo en 65 869 mujeres posmenopáusicas (WHI-OS) en el que se evaluó la periodontitis por autorreferencia, existía una asociación estadísticamente significativa con el riesgo de padecer cáncer total (MVR 14 %; IC 95 %: 1,14; 1,08-1,20), y también asociaciones positivas para cánceres de esófago, mama, pulmón, vesícula biliar y piel tipo melanoma (Nwizu y cols. 2017). En el Estudio de Seguimiento de Profesionales de la Salud (HPFS), evaluando hombres (n = 19 933) que nunca habían fumado, la periodontitis autorreferida se asoció con un aumento del 13 % del riesgo total de cáncer (IC 95 % de la MVR: 1,13; 1,01-1,27). Dicho riesgo fue más pronunciado en hombres con periodontitis avanzada (45 %) (aquellos con <17 dientes restantes) (Michaud y cols. 2016).
En el Estudio de Riesgo de Aterosclerosis en Comunidades (ARIC), que analiza una cohorte de 7466 sujetos en los que se evaluó la periodontitis mediante un examen periodontal completo y se controlaron los factores de confusión incluyendo el tabaquismo, los sujetos con periodontitis severa (>30 % de localizaciones con pérdida de inserción >3 mm) tenían un riesgo total de cáncer elevado del 24 %, en comparación con aquellos sin periodontitis o con periodontitis leve (<10 % de los sitios con pérdida de inserción >3 mm) (Michaud y cols. 2018). Igualmente, en un registro de 68 273 adultos de Helsinki seguidos durante un periodo de 10 años, la periodontitis se asoció con una mayor mortalidad por cáncer en general (RR IC 95 %: 1,33; 1,10-1,58) y especialmente con la mortalidad por cáncer de páncreas (RR IC 95 %: 1,69; 1,04-2,76) (Heikkila y cols. 2018).
Las diferencias observadas entre los estudios pueden explicarse por la imprecisa evaluación de la exposición (periodontitis), ya que, en muchos de ellos, la evaluación de la exposición se realizó por la autorreferencia del paciente o el estado de pérdida de sus dientes; además, el grado de control para factores de riesgo compartidos, sobre todo el tabaquismo, no se realizó de un modo homogéneo.
Enfermedad periodontal y riesgo de cáncer de cabeza y cuello
La asociación entre periodontitis y riesgo de cáncer de cabeza y cuello, especialmente los cánceres de la cavidad oral y orofaringe, ha sido la más ampliamente explorada. La mayoría de los estudios presentan una asociación significativa, especialmente con el cáncer oral, en particular en estudios realizados en EE. UU. (Graham y cols. 1977), Europa (Lissowska y cols. 2003), América Latina (Guha y cols. 2007), India (Subapryya y cols. 2007), China (Zheng y cols. 1990) y Brasil (Velly y cols. 1998).
En el estudio NHANES III, con una muestra de 13 798 adultos, la pérdida de inserción clínica media (≥1,5 mm) se asoció con un mayor riesgo general de tumores orales (OR IC 95 %: 4,57; 2,25-9,30), después de ajustar muchos factores de confusión, incluidos el tabaquismo y el alcohol (Tezal y cols. 2005). Otro estudio de casos y controles que incluía 200 casos de cáncer oral/orofaríngeo y 200 controles reportó una asociación estadísticamente significativa entre el número de dientes perdidos (≥16 dientes) y los casos de cáncer oral/ orofaríngeo (OR IC 95 %: 2,74; 1,23-6,12) (Garrote y cols. 2001). En un estudio de 1361 casos y 1289 controles describieron que la movilidad dental se asociaba positivamente con el carcinoma de células escamosas de cabeza y cuello (OR IC 95 %: 1,33; 1,07-1,65) después de controlar los posibles factores de confusión. Sin embargo, la pérdida de dientes (16-28 dientes perdidos frente a 0-5 dientes perdidos) no se asoció con el riesgo de cáncer (Divaris y cols. 2009).
En los últimos años distintas revisiones sistemáticas, algunas incluyendo metaanálisis, han agrupado los estudios que han valorado estas asociaciones. Zeng y cols. (2013) analizaron 2 estudios de cohortes y 6 estudios de casos y controles. La exposición se estudió mediante pérdida ósea alveolar (3 estudios), pérdida de inserción clínica (1 estudio), índice periodontal comunitario de necesidades de tratamiento (CPITN) (1 estudio), movilidad dental (1 estudio) y mala condición bucal (1 estudio). Los resultados del metaanálisis revelaron una asociación estadísticamente significativa entre periodontitis y el riesgo de cáncer de cabeza y cuello (OR IC 95 %: 2,63; 1,68-4,14) (Zeng y cols. 2013). Más recientemente, los mismos autores han publicado una nueva revisión sistemática con metaanálisis que incluye 1 estudio de cohortes y 10 estudios de casos y controles, reportando igualmente un riesgo significativamente mayor de cáncer de cabeza y cuello (OR IC 95 %: 1,58; 1,08-2,32) entre los participantes que habían perdido entre 6 y 15 dientes, siendo el riesgo progresivamente más alto con una pérdida mayor de 15 dientes (Zeng y cols. 2013).
En otra publicación reciente realizando metarregresión en 7 estudios de casos y controles, se reportó una relación lineal entre el número de dientes perdidos y el riesgo de cáncer bucal. Por cada diente perdido adicional, la odds ratio aumentó significativamente en 0,03 (IC 95 %: 0,01-0,05), aunque se observó una heterogeneidad moderada (I2 = 67,5 %, P = 0,003) (Michaud y cols. 2017).
Entre los estudios epidemiológicos publicados de mayor tamaño muestral, uno se realizó en Taiwán sobre una cohorte de 148 166 sujetos, demostrándose una asociación positiva entre la periodontitis y el cáncer bucal (HR IC 95 %: 1,20; 1,09-1,33) (Chung y cols. 2016). Sin embargo, en una cohorte de 65 869 mujeres de edad avanzada en EE. UU. no se demostró una asociación significativa entre periodontitis autorreferida y cánceres de labio, cavidad oral y faringe combinados (HR IC 95 %: 1,10; 0,64-1,87) (Nwizu y cols. 2017).
Los cánceres de cabeza y cuello comprenden un grupo heterogéneo de procesos oncológicos asociados a distintos factores de riesgo, sobre todo al tabaquismo y el consumo de alcohol.
Por tanto, el estudio de su asociación a periodontitis presenta dificultades, no solo por la gran discrepancia en la prevalencia y patocronía de ambas enfermedades, sino por las dificultades en el control adecuado de los factores de confusión y factores de riesgo compartido, lo que exige estudios de casos y controles de tamaños muestrales muy grandes, ya que los estudios prospectivos de cohortes son muy difíciles de realizar, lo que dificulta aún más determinar la posible causalidad de la posible asociación. En resumen, la evidencia científica apunta hacia una asociación positiva entre periodontitis y el riesgo de cáncer de cabeza y cuello.
Enfermedad periodontal y riesgo de cáncer de pulmón
El riesgo de cáncer de pulmón en relación con la periodontitis presenta el problema del ajuste con el tabaquismo, que es el mayor factor de riesgo de este tipo de cáncer. Por ejemplo, en el estudio epidemiológico NHANES, al ajustar el tabaquismo, aunque el riesgo de mortalidad por cáncer de pulmón se mantuvo significativo en los sujetos con periodontitis (OR IC 95 %: 1,73; 1,01-2,97), se observaron estimaciones de riesgo opuestas cuando se comparó la asociación entre los fumadores (OR IC 95 %: 1,94; 1,14-3,30) y los nunca fumadores (OR IC 95 %: 0,58; 0,12-2,78) (Hujoel y cols. 2013). Recientemente, las estimaciones de un metaanálisis basado en la evaluación de cinco estudios de cohortes asociaron un mayor riesgo de cáncer de pulmón en pacientes con periodontitis (HR IC 95 %: 1,24; 1,13-1,36; P para heterogeneidad = 0,22). Estos resultados, sin embargo, deben interpretarse con cautela, ya que los estudios incluidos han evaluado la exposición (periodontitis) utilizando distintos métodos (Michaud y cols. 2017). En un reciente estudio se asoció significativamente la periodontitis severa con un mayor riesgo de cáncer de pulmón y bronquios (HR IC 95 %: 2,37; 1,41-3,99), describiéndose que los pacientes de raza blanca tenían un riesgo ligeramente mayor (HR IC 95 %: 2,36; 1,27-4,39) en comparación con los pacientes de raza negra (HR IC 95 %: 2,20; 0,83-5,78) (Michaud y cols. 2018).
En general, la evidencia científica sugiere un posible efecto sinérgico entre la periodontitis y el tabaquismo en relación con el riesgo de cáncer de pulmón, aunque no se conoce con precisión la asociación entre periodontitis y el riesgo de incidencia o mortalidad por cáncer de pulmón en no fumadores.
Enfermedad periodontal y riesgo de cánceres del tracto digestivo
Varios estudios han valorado la asociación entre periodontitis y los distintos cánceres del tracto digestivo. En un estudio de adultos sanos de zonas rurales de China (n = 29 584) se asoció significativamente una mayor pérdida de dientes con el riesgo de mortalidad por cáncer gastrointestinal superior (n = 2625 muertes) (HR IC 95 %: 1,35; 1,14-1,59), y este aumento no se limitó solo a los fumadores. En el estudio NHANES III sobre 12 605 hombres y mujeres el riesgo de mortalidad por cáncer orodigestivo estaba significativamente asociado con la periodontitis moderada/grave, y dicho riesgo aumentó con una mayor severidad de la periodontitis (RR IC 95 %: 2,28; 1,17-4,45; Ptrend = 0,01) (Ahn y cols. 2012).
Un estudio más reciente en el que participaron ancianos japoneses encontró una asociación positiva entre la pérdida de dientes y la mortalidad por cáncer orodigestivo (Ansai y cols. 2013). La mayoría de los estudios existentes evidencian una asociación positiva entre la periodontitis y el cáncer orodigestivo/gastrointestinal superior, aunque basada más en la pérdida dentaria que en la incidencia de periodontitis.
Igualmente, se ha descrito un mayor riesgo de cáncer de esófago en pacientes con afectación periodontal (Abnet y cols. 2001; Abnet y cols. 2008; Dye y cols. 2007; Hiraki y cols. 2008), aunque la mayoría evalúan la pérdida de dientes como una medida indirecta de severidad en la afectación periodontal. Por ejemplo, en un estudio realizado en China se describió una asociación significativa entre cáncer de esófago y la pérdida de dientes (RR IC 95 %: 1,3; 1,1-1,6) (Abnet y cols. 2001). Sin embargo, un estudio similar realizado en Finlandia no encontró ninguna asociación entre periodontitis y cánceres de esófago (subtipos carcinoma de células escamosas o adenocarcinoma) (Abnet y cols. 2005).
Revisiones sistemáticas recientes con metaanálisis agrupando ocho estudios (cohorte, n = 3; caso-control, n = 5), todos ellos ajustados para múltiples factores de confusión, incluido el tabaquismo, mostraron un riesgo elevado de cáncer de esófago (OR IC 95 %: 1,36; 1,16-1,59; I2 = 0) entre aquellos con mayor pérdida de dientes (Chen y cols. 2015). En otro metaanálisis más reciente a partir de tres estudios de cohortes, cinco estudios de casos y controles y un estudio transversal, la pérdida de dientes también se relacionó positivamente con un mayor riesgo de cáncer de esófago (RR IC 95 %: 1,30; 1,06-1,60; I2 = 13,5 %), observándose una relación dosis-respuesta significativa (RR IC 95 %: 1,01; 1,00-1,03) (Chen y cols. 2016).
Estos estudios disponibles, especialmente los estudios epidemiológicos más recientes, indican una asociación positiva entre cánceres de esófago y pacientes con periodontitis, manteniéndose el riesgo en los pacientes no fumadores.
La evidencia epidemiológica de la asociación entre la enfermedad periodontal y el cáncer gástrico muestra resultados variados. Una revisión sistemática en 2016 combinando cinco estudios de cohortes y cuatro estudios de casos y controles concluyó que la pérdida de dientes puede estar relacionada con el cáncer gástrico (estudios de cohortes combinados RR IC 95 %: 1,31; 1,12-1,53; estudios de casos y controles combinados RR IC 95 %: 1,86; 1,08-3,21) (Shakeri y cols. 2013). Sin embargo, un estudio de casos y controles en Irán no encontró asociación entre las subcategorías de pérdida de dientes y el riesgo de adenocarcinomas gástricos en general, y entre sus subtipos histológicos, adenocarcinoma gástrico de cardias y adenocarcinoma gástrico no de cardias (Yin y cols. 2016). Por lo tanto, la evidencia disponible no permite concluir que existe una asociación entre periodontitis y los cánceres gástricos, si es que existe.
Sin embargo, sí existe evidencia epidemiológica de asociación significativa entre periodontitis y cáncer de páncreas. En un estudio de 29 104 sujetos finlandeses de sexo masculino, en que se utilizó la pérdida de dientes como medida indirecta de periodontitis, sí se encontró asociación significativa (HR IC 95 %: 1,63; 1,09-2,46; tendencia P = 0,02) (Stolzenberg-Solomon y cols. 2003). Igualmente, se han descrito asociaciones positivas similares en una cohorte en Suecia de 15 333 individuos (HORA IC 95 %: 2,06; 1,14-3,75) (Arora y cols. 2010) y otra en EE. UU. de 51 529 profesionales sanitarios varones (RR IC 95 %: 1,64; 1,19-2,26) (Michaud y cols. 2007). Se ha observado en estos estudios un mayor riesgo de desarrollar cáncer de páncreas con una mayor severidad de periodontitis (RR IC 95 %: 2,7; 1,70-4,32). Sin embargo, Hiraki y cols. (2013) no encontraron asociación entre periodontitis y el riesgo de cáncer de páncreas en su estudio de casos y controles de 15 720 participantes con 178 casos de cáncer de páncreas.
En un estudio reciente en Taiwán evaluando a 214 890 personas con 107 casos de cáncer de páncreas se encontró un mayor riesgo entre aquellos con evidencia de periodontitis registrada en la base de datos nacional (HR IC 95 %: 1,55; 1,02-2,33). El riesgo de cáncer de páncreas fue más pronunciado entre aquellos ≥65 años (HR IC 95 %: 2,17; 1,03-4,57) (Chang y cols. 2016). Un estudio de cohortes independiente de 19 924 participantes suecos con 126 casos registrados de cáncer de páncreas mostró un riesgo aumentado, pero no significativo, de cáncer de páncreas entre las personas con 0 a 10 dientes (HR IC 95 %: 1,3; 0,7-2,3), u 11-20 dientes (HR IC 95 %: 1,2; 0,7-2,0), en comparación con aquellos con ≥21 dientes, respectivamente (Huang y cols. 2016). Sin embargo, la mala higiene bucal en individuos con menos de 10 dientes se asoció con un riesgo marcadamente elevado de cáncer de páncreas (HR IC 95 %: 2,0; 1,0-4,1) tras ajustar por factores de confusión importantes, incluidos antecedentes de tabaquismo y consumo de alcohol.
Una revisión sistemática publicada en 2017 que incluía ocho estudios corroboró que la periodontitis está relacionada con el riesgo de cáncer de páncreas (RR IC 95 %: 1,74; 1,41- 2,15) (Maisonneuve y cols. 2017).
Con respecto a los estudios sobre la mortalidad por cáncer de páncreas, los resultados son discrepantes, ya que mientras un estudio en ancianos japoneses (n = 656) no encontró ninguna asociación entre la periodontitis y el riesgo de mortalidad por cáncer de páncreas (HR IC 95 %: 0,96; 0,83-1,11) (Ansai y cols. 2013), en un estudio (n = 68 273) de Helsinki con 75 casos de cáncer de páncreas se observó un riesgo de mortalidad por cáncer de
páncreas más del doble. Sin embargo, en este estudio no se controlaron los factores de riesgo relacionados con el tabaquismo y el alcohol (Heikkila y cols. 2018).
Aunque no se ha demostrado una asociación evidente entre periodontitis y el riesgo de cáncer de páncreas, el hecho de que la periodontitis se haya asociado significativamente con el riesgo de este tipo de cáncer entre personas que nunca han fumado puede ser una indicación de una asociación independiente, que debería explorarse más a fondo.
Los estudios sobre la relación entre la enfermedad periodontal y el riesgo de cáncer colorrectal, aunque limitados en número, en su mayoría apuntan a la ausencia de una asociación. La cohorte HPFS no encontró ningún vínculo entre el riesgo de cáncer colorrectal y la enfermedad periodontal autodeclarada (HR IC 95 %: 1,05; 0,90-1,23), o la pérdida de dientes (0-16 dientes restantes) (HR IC 95 %: 1,10; 0,87-1,37), después de los ajustes por tabaquismo y otros factores de confusión importantes (Michaud y cols. 2008).
Igualmente, el estudio de seguimiento NHANES I que utiliza medidas clínicas para evaluar la periodontitis no encontró asociación con el riesgo de mortalidad por cáncer de colon (OR IC 95 %: 0,91; 0,49-1,70) (Hujoel y cols. 2003), aunque el estudio NHANES III mostró un riesgo significativamente elevado de muerte por cáncer colorrectal (RR IC 95 %: 3,58; 1,15-11,16) (Ahn y cols. 2012). El único estudio con resultados significativos entre periodontitis y cáncer colorrectal (62 %) corresponde a una cohorte sueca de 15 333 gemelos (HR IC 95 %: 1,62; 1,13-2,33) (Arora y cols. 2010). En este trabajo los resultados fueron ajustados a los factores de riesgo de cáncer a nivel individual y a los posibles factores de confusión. Una revisión sistemática publicada en 2017 agrupando cuatro estudios de cohortes (Michaud y cols. 2017) mostró un riesgo elevado, pero no significativo, evidenciando resultados muy dispares entre los estudios (RR IC 95 %: 1,47; 0,95-2,29; I2 = 66,5 %; P = 0,03). Con los datos de los que disponemos en la actualidad no se puede concluir que exista una asociación significativa entre periodontitis y el cáncer colorrectal.
La asociación entre periodontitis y cáncer de mama tampoco ha podido ser demostrada con claridad. El grupo de Michaud, utilizando medidas clínicas para evaluar periodontitis (definición de los CDC/AAP) en sujetos no fumadores, no encontró una asociación significativa con el riesgo de cáncer de mama (Michaud y cols. 2018). Sin embargo, en una cohorte retrospectiva basada en 40 206 mujeres, con igual número de casos y controles emparejados, y 267 casos de cáncer de mama notificados, la tasa de cáncer de mama fue significativamente mayor entre las mujeres con periodontitis que en la cohorte control (HR IC 95 %: 1,23; 1,11-1,36) (Chung y cols. 2016).
En la relación entre periodontitis y el riesgo de cáncer de mama, el tabaquismo y quizá otros factores de confusión no tan evidente pueden ser los factores que expliquen la asociación significativa en algunos estudios.
En otros tipos de cáncer, los datos epidemiológicos publicados son muy escasos. Por ejemplo, en relación con el riesgo de cáncer de vesícula biliar, tan solo existe un estudio con una muestra relativamente baja (n = 60) en el que los pacientes con periodontitis tuvieron un riesgo estadísticamente significativo de ser diagnosticados de este tipo de cáncer (HR IC 95 %: 1,73; 1,01-2,95). Sin embargo, al restringirlo a los nunca fumadores la asociación se redujo notablemente (HR IC 95 %: 1,26; 0,59-2,68) (Nwizu y cols. 2017).
En cáncer de hígado, en cáncer de próstata, cánceres de vías urinarias y cánceres hematológicos, existen estudios dispares que presentan alguna asociación positiva con periodontitis, aunque la mayor parte de los estudios existentes no han encontrado un mayor riesgo de padecer estos tipos de cáncer en pacientes con periodontitis.
Estudios de intervención que evalúan el tratamiento de la periodontitis y el riesgo de cáncer
No existen ensayos clínicos controlados aleatorios sobre el tratamiento de la periodontitis y el riesgo de cáncer, pero se han publicado algunos estudios de asociación. Uno de estos trabajos investigó los efectos del tratamiento rutinario de las enfermedades periodontales sobre el riesgo de cáncer utilizando datos del sistema de Seguro Nacional de Salud (NHI, por sus siglas en inglés) de Taiwán. La cohorte de tratamiento comprendía 38 902 participantes, a los que se les había diagnosticado periodontitis y habían recibido al menos 10 tratamientos, incluido el raspado y alisado radicular y la cirugía de colgajo periodontal. La cohorte de comparación estaba compuesta por 77 804 participantes, en la que se seleccionaron aleatoriamente dos individuos de la misma edad y sexo para cada miembro de la cohorte de tratamiento (Hwang y cols. 2014). Dicha cohorte de tratamiento de periodontitis mostró una marcada reducción en el riesgo general de cáncer (HR IC 95 %: 0,72; 0,68-0,76) en relación con la cohorte de control. El riesgo de cáncer de esófago (HR IC 95 %: 0,20; 0,12-0,34), colon/ recto (HR IC 95 %: 0,70; 0,60-0,82), pulmón (HR IC 95 %: 0,45; 0,38-0,54), tracto reproductivo femenino (HR IC 95 %: 0,58; 0,46-0,72) y cerebro (HR IC 95 %: 0,35; 0,18-0,67) se redujo de manera similar. Por el contrario, los riesgos de cáncer de próstata (HR IC 95 %: 2,11; 1,63-2,73) y de tiroides aumentaron significativamente en la cohorte de tratamiento. No se realizaron ajustes para factores de confusión como el tabaquismo, el consumo de alcohol y otras características de estilo de vida y comportamiento.
El estudio de Moergel y cols. (2013) reporta que una historia de tratamiento periodontal está inversamente asociada con el riesgo de cáncer oral (OR IC 95 %: 0,2; 0,1-0,5), y, en la misma línea, Chung y cols. (2016) encontraron que el riesgo de cáncer aumentó significativamente entre los participantes con periodontitis que no recibieron ningún tratamiento periodontal, en comparación con aquellos que no tenían periodontitis (HR IC 95 %: 1,29; 1,21-1,32). Sin embargo, no observaron diferencias significativas en el riesgo de cáncer entre los participantes con periodontitis que recibieron tratamiento (gingivectomía u operación de colgajo periodontal) en relación con la cohorte de comparación sin enfermedad periodontal (HR IC 95 %: 1,17; 0,86-1,58).
Dado que la evidencia sobre el tratamiento de la enfermedad periodontal y el riesgo de cáncer se ha basado en estudios observacionales y no en ensayos clínicos controlados aleatorios, dicha evidencia está sujeta a los mismos sesgos y problemas relacionados con la posible falta de ajuste de factores de confusión, por lo que es necesario profundizar en el papel que el tratamiento periodontal puede tener en el riesgo de cáncer.
Posibles mecanismos que expliquen la asociación entre periodontitis y riesgo de cáncer
Se han propuesto varios mecanismos plausibles, siendo la inflamación sistémica el mecanismo más reportado en la literatura. Es evidente que la periodontitis supone una fuente constante de inflamación sistémica crónica de baja intensidad si no se trata.
Igualmente, es palmaria la relación de inflamación sistémica y cáncer (Balkwill y cols. 2001; Coussens y cols. 2002; Mantovani y cols. 2008). Los procesos inflamatorios crónicos generan radicales libres que causan estrés oxidativo/nitrosativo, lo que conduce a mutaciones del ADN celular o pueden interferir con los mecanismos de reparación del ADN (Federico y cols. 2007). Igualmente, altos niveles séricos de citocinas, quimiocinas y metabolitos del ácido araquidónico estimulan la liberación por el hígado de proteína C reactiva y otras proteínas que perpetúan la inflamación sistémica (Federico y cols. 2007).
De la misma manera, bacterias anaeróbicas gramnegativas presentes en alta proporción en el biofilm subgingival de pacientes con periodontitis, como Porphyromonas gingivalis y Aggregatibacter actinomycetemcomitans (Page 1998), tienen capacidad por sí mismas o sus toxinas de invadir los tejidos, pasar al plasma y distribuirse por todo el organismo y causar daño directo al ADN celular, pudiendo inducir mutaciones en protooncogenes y genes supresores de tumores, o interferir con las vías moleculares involucradas en la proliferación y/o supervivencia celular (Anil y cols. 2012).
A nivel de la cavidad oral (Pushalkar y cols. 2012), las bacterias orales pueden promover la carcinogénesis al activar los receptores TLR (como el TLR-5) presentes en las superficies de las células del sistema inmune innato, células epiteliales y cancerosas (Kauppila y cols. 2013a; Kauppila y cols. 2013b).
Se han aislado patógenos periodontales como Fusobacterium nucleatum, tanto en enfermedades inflamatorias del intestino como la enfermedad de Crohn (Dharmani y cols. 2011) o colitis ulcerosa (Strauss y cols. 2011), como en lesiones premalignas tales como adenomas colorrectales (Kostic y cols. 2013) y cáncer colorrectal (Castellarin y cols. 2012; Kostic y cols. 2012). Rubinstein y cols. (2013) demostraron que Fusobacterium nucleatum a través de una molécula de adhesión FadA puede adherirse y penetrar en el epitelio del colon y puede desregular dichas células, favoreciendo la proliferación de células de cáncer colorrectal a través de sus propiedades. Kostic y cols. (2013), en modelos experimentales murinos de ratón (ratones Apc (Min/+)), han demostrado que Fusobacterium nucleatum puede atraer específicamente células mieloides que se infiltran en tumores y crear un entorno proinflamatorio que promueve la carcinogénesis colorrectal. Además, se ha demostrado que Fusobacterium nucleatum tiene capacidad de modular el sistema inmune antitumoral (Kostic y cols. 2013) y promover la progresión tumoral al suprimir las células T citotóxicas y efectoras.
Igualmente, Peters y cols. (2017) han demostrado que el patógeno periodontal Tannerella forsythia está asociado con el adenocarcinoma esofágico. También se ha descrito una asociación entre el patógeno Porphyromonas gingivalis y el riesgo de carcinoma esofágico de células escamosas (Peters y cols. 2017). Gao y cols. (2016) reportaron que Porphyromonas gingivalis se encontraba en el 61 % de muestras de tejidos de pacientes con carcinoma esofágico de células escamosas, pero no se detectó en la mucosa esofágica normal.
La hipótesis de que las bacterias anaerobias gramnegativas presentes en gran número en el biofilm subgingival de pacientes con periodontitis sean microaspiradas, ingeridas, o en bacteriemias distribuirse por vía sanguínea a órganos o regiones distantes donde puedan colonizar y causar patología ha sido avalada por múltiples estudios que han aislado patógenos periodontales en muchas partes del cuerpo además de la cavidad oral, incluidas las placas ateromatosas de los vasos sanguíneos (Gaetti-Jardim y cols. 2009; Haratszthy y cols. 2000; Padilla y cols. 2008), ganglios linfáticos (Amodini Rajakaruna y cols. 2012), aspirados pulmonares (Barlett y cols. 1974; Goldstein y cols. 1979), líquido pericárdico (Truant y cols. 1983), tejidos del hígado (Yoneda y cols. 2012), infecciones de la columna vertebral (Le Moal y cols. 2005), amígdalas (Brook y cols. 1994), y el apéndice vermiforme (Swidsinski y cols. 2011). Aunque la liberación de estas bacterias orales en el torrente sanguíneo es temporal, los patógenos periodontales como Porphyromonas gingivalis pueden evadir su absorción y destrucción por los fagocitos a través de su producción de proteasas, como las gingipaínas (Cutler y cols. 1993), y de este modo evitar su destrucción (Mege y cols. 2011; Pulendran y cols. 2001). Por otro lado, se ha demostrado que las células dendríticas fagocitan, pero no destruyen, los microorganismos Porphyromonas gingivalis, permitiendo así que estas células bacterianas intracelulares lleguen a órganos distantes y de este modo producir sus efectos nocivos a distancia (Carrion y cols. 2012).
De hecho, se han encontrado microorganismos orales en lesiones precancerosas del estómago (Salazar y cols. 2013), del colon (Kostic y cols. 2013) y ciertos tipos de cáncer, como el carcinoma colorrectal (Castellarin y cols. 2012; Kostic y cols. 2012), carcinomas orales (Sasaki y cols. 2005), y cánceres de esófago y de estómago (Narikiyo y cols. 2004; Sasaki y cols. 1998).
La periodontitis además se asocia frecuentemente a diabetes, lo que puede influir sobre su sistema inmunológico, particularmente en lo que respecta a la eliminación de bacterias y la vigilancia inmunológica de los tumores (Myer y cols. 2008), pudiendo aumentar su susceptibilidad al cáncer. En estados de hiperglucemia, la formación de AGE (productos finales de la glicación avanzada) actuando a nivel celular se ha relacionado tanto con inflamación crónica como con el cáncer (Lalla y cols. 2001; Logsdon y cols. 2007).
La periodontitis avanzada se asocia a pérdida de dientes, lo que puede influir en la eficiencia masticatoria y secundariamente en la nutrición de los pacientes (Chauncey y cols. 1984; Wallas y cols. 2000). Distintos estudios han demostrado que las frutas y las verduras sin almidón están asociadas con un menor riesgo de ciertos tipos de cáncer (cavidad oral, faringe, esófago, estómago y pulmón) (World Cancer Research Fund 2007). Sin embargo, las dietas hipercalóricas se comportan como proinflamatorias con niveles más elevados de PCR e IL-6, lo que puede promover el riesgo de cáncer (Mazul y cols. 2018; Namazi y cols. 2018; Shivappa y cols. 2014). Finalmente, los cambios epigenéticos que resultan en hipermetilación de E-cadherina y ciclooxigenasa-2 se han asociado con la periodontitis crónica y pueden estar vinculados con un mayor riesgo de cáncer (Loo y cols. 2010).
En la Figura 2 se resumen las rutas propuestas para el armazón de la periodontitis en relación con las características distintivas y facilitadoras del cáncer.
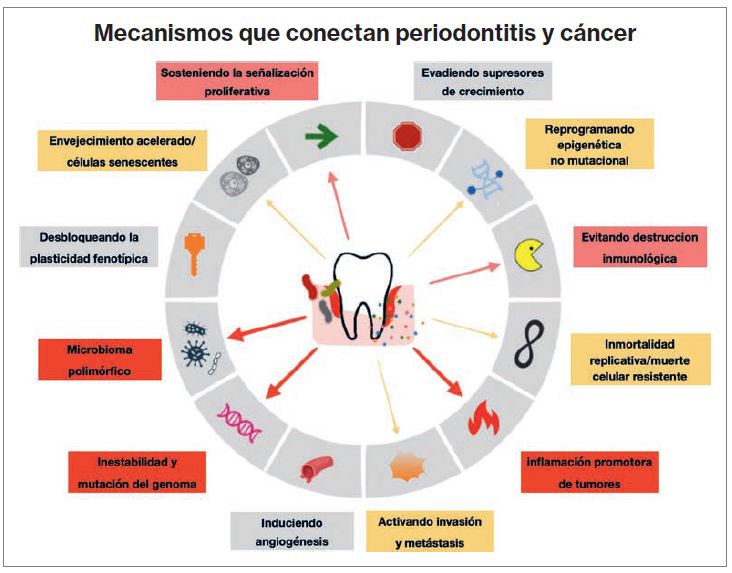
Figura 2. Rutas propuestas para el armazón de la periodontitis en relación con las características distintivas y facilitadoras del cáncer. La presencia y el grosor de las flechas reflejan la cantidad de evidencia disponible. (Modificado de Hanahan 2022).
LOS PACIENTES CON CÁNCER Y PERIODONTITIS. CUESTIONES PRÁCTICAS
POR SU PROPIA NATURALEZA, la periodontitis y su tratamiento pueden condicionar y complicar la situación oral y general del paciente con cáncer, así como su terapia adecuada, por lo que es necesario analizar con el oncólogo la condición sistémica del paciente, su estado de inmunosupresión y la premura en instaurar el tratamiento oncológico, algo que puede modificar notablemente el abordaje periodontal previo. En esta sección, y debido a su extensión limitada, se describen fundamentalmente situaciones para tener en cuenta en el manejo periodontal del paciente con cáncer.
Prácticas de higiene y cuidado bucal para el paciente oncológico en todas las fases de su proceso terapéutico
Es esencial la motivación y una higiene bucal cuidadosa en todas las fases del tratamiento del cáncer para reducir la incidencia y la gravedad de los efectos adversos bucales de la terapia oncológica (NCI 2024; Rankin y cols. 2009).
Se debe utilizar un cepillo de dientes suave, pudiendo ser eléctrico si no causa traumatismos. La limpieza interdental atraumática se debe realizar 1 vez al día. La pasta de dientes con flúor de sabor suave se utilizará 2 veces al día, enjuagándose con frecuencia. Los productos en gel con flúor (fluoruro de sodio neutro al 1,1 % o fluoruro de estaño sin sabor al 0,4 %) se pueden utilizar 1 vez al día durante 2 a 3 minutos. Si no se tolera la pasta de dientes se puede utilizar en su lugar solución salina al 0,9 %, o agua. En los casos en que no sea posible el cepillado dental se pueden utilizar enjuagues antimicrobianos, por ejemplo, clorhexidina sin alcohol. Si no es bien tolerada, se puede recomendar enjuagues con soluciones saturadas de bicarbonato o solución salina al 0,9 %, pudiéndose utilizar cada 2 a 4 horas o según sea necesario para aliviar las molestias en la boca. Existe un buen número de pautas de higiene y cuidado bucodental para tipos de situaciones más específicas, como mucositis, xerostomía, disgeusia, etc. (Decker y cols. 2018).
Pacientes periodontales que van a comenzar un tratamiento antineoplásico
Según el Instituto Nacional del Cáncer (NCI, por sus siglas en inglés), no existe un protocolo dental/periodontal de terapia precancerosa universalmente aceptado, debido a la falta de ensayos clínicos reglados que evalúen su eficacia (National Cancer Institute 2024).
No obstante, se han publicado varios estudios que pueden orientar en este sentido (Brennan y cols. 2008; Decker y cols. 2018; Hong y cols. 2017).
¿Cuándo es aconsejable intervenir a nivel periodontal?
Idealmente, los pacientes deberían consultar con su dentista 4 semanas antes de iniciar el tratamiento oncológico (si esta situación es posible) con el fin de permitir un manejo de los tejidos periodontales con ciertas garantías si se requiere algún tratamiento periodontal. Cuando sea necesario, se deben realizar extracciones cerrando el tejido con suturas independientes para lograr una rápida cicatrización. En el caso de los tumores de cabeza y cuello es recomendable realizar estos procedimientos al menos 3 semanas antes del inicio de la radioterapia en dientes retenidos sintomáticos, y entre 10 y 14 días antes si el diente a extraer no es complicado y se encuentra en la zona a irradiar que se espera reciba una dosis de al menos 50 Gy, o en un tiempo menor si el diente a extraer se encuentra fuera del área afectada por la radioterapia. Todo lo anterior pretende minimizar el riesgo de osteorradionecrosis de los maxilares (Hong y cols. 2018). Los pacientes que van a recibir quimioterapia, especialmente cuando incluye tratamiento antirresortivo, antiangiogénico o con ciertos inmunomoduladores, requieren de una evaluación cuidadosa debido al riesgo de desencadenar osteonecrosis relacionada con medicamentos por procedimientos de extracciones o quirúrgicos (Ruggiero y cols. 2014).
¿Qué medidas generales se pueden tomar?
Las características generales de la evaluación y el cuidado periodontal previos al tratamiento oncológico pueden incluir, además de las esenciales instrucciones en higiene oral (Rankin y cols. 2009):
• Examen periodontal mediante estudio clínico y radiológico indicados. Buscar restos radiculares retenidos.
• Eliminación de posibles fuentes de traumatismo intraoral, como restauraciones afiladas, dientes rotos, prótesis o aparatos de ortodoncia mal ajustados, etc.
• Planificación y reducción del riesgo de posibles efectos adversos bucales, incluyendo infecciones, deterioro nutricional, dolor, mucositis, xerostomía, etc. Educar a los pacientes en la importancia de estos aspectos.
¿Qué se puede hacer a nivel periodontal?
Una revisión sistemática reciente desarrolló pautas para el manejo de la caries dental, la enfermedad periodontal y las infecciones dentales en pacientes con cáncer con los criterios siguientes (Kurita y cols. 2024):
• Si el tiempo y el estado general del paciente sí lo permiten, se debe realizar el tratamiento periodontal no quirúrgico (pasos 1 y 2) antes del tratamiento del cáncer, siempre con el control de la higiene oral y de los factores de riesgo periodontales.
• Si se anticipa un estado inmunodeprimido, sería aconsejable realizar el tratamiento periodontal de acuerdo con los siguientes criterios:
– La infección periodontal sintomática aguda y grave debe tratarse mediante extracción y/o medios farmacológicos.
– Si la profundidad de sondaje es mayor de 8 mm y la movilidad es de grado III, se debe extraer el diente.
– Los pacientes asintomáticos periodontalmente con una profundidad de sondaje menor de 8 mm y una movilidad de grado II o menor pueden ser objeto de seguimiento tras realizarse el tratamiento periodontal básico.
• Si el tiempo y el estado general del paciente no permiten una terapia periodontal previa adecuada, el manejo de las infecciones sintomáticas agudas y graves debe realizarse de todos modos antes o junto con el tratamiento del cáncer.
Pacientes periodontales que están en tratamiento oncológico activo
Es importante resaltar que la prevalencia de la enfermedad periodontal en una población oncológica fue del 35,2 % en el momento de su diagnóstico de cáncer, con el riesgo sistémico que esto comporta (Vozza y cols. 2015). Esta prevalencia no difiere de la observada en la población no oncológica (Carasol y cols. 2016), por lo que es importante insistir en la necesidad de prevención y tratamiento temprano de las enfermedades periodontales para evitar complicaciones ante la necesidad de abordar la terapia oncológica.
En esta fase es imprescindible conocer detalladamente la situación del paciente, sus tratamientos antineoplásicos y generales, así como su capacidad para someterse a un tratamiento periodontal en función del estado hematológico (Massler y cols. 2000).
Una de las principales y frecuentes complicaciones de los tratamientos quimioterápicos es la neutropenia; hay autores que concluyen que, cuando el recuento de neutrófilos sea <500 mm3, cualquier procedimiento dental/periodontal está estrictamente desaconsejado (Hong y cols. 2018). Si el sondaje o el tratamiento son necesarios se debería esperar a la recuperación de la neutropenia o utilizar factores de crecimiento de colonias hematopoyéticas, que suelen restaurar la cifra de neutrófilos en unas 48-72 horas, junto con una cobertura antibiótica adecuada para permitir la manipulación periodontal sin riesgo.
Puede ser apropiado considerar con los oncólogos protocolos de profilaxis antibiótica empírica antes de procedimientos periodontales invasivos en personas que tienen dispositivos de acceso vascular implantados, catéteres venosos centrales, etc. (Brennan y cols. 2008).
Lo mismo ocurre con la trombopenia inducida por los antineoplásicos, sobre todo cuando la cifra de plaquetas baja de 20 000 con un riesgo hemorrágico muy alto a pesar de la hemostasia cuidadosa, pudiendo ser necesario transfundir plaquetas antes de la manipulación periodontal.
Es importante saber si el paciente está recibiendo fármacos antirresortivos con efecto antiangiogénico o inhibidores de la tirosina quinasa, ya que unos bloquean los factores de crecimiento vascular impidiendo la angiogénesis, por lo que la cicatrización de los tejidos se puede comprometer durante los tratamientos periodontales, y otros conllevan un riesgo de inducir osteonecrosis mandibular (Decker y cols. 2018).
La gingivitis puede tratarse durante la terapia oncológica, excepto en las fases de neutropenia. Hay que tener en cuenta que puede verse afectada por el estado hematológico, pudiendo estar pálida en casos de anemia, eritematosa en el paciente trombocitopénico (Philipone y cols. 2023), o agrandada en pacientes con leucemia mieloide aguda (Lowenberg y cols. 1999).
La periodontitis se puede abordar mediante tratamiento no quirúrgico y se ha mostrado eficaz para reducir el índice de placa, el sangrado al sondaje, la profundidad de la bolsa y el mantenimiento de la pérdida de inserción mientras los pacientes estudiados se sometían a quimioterapia (Decker y cols. 2018).
Cuando un paciente con periodontitis desarrolla fiebre neutropénica, si es posible se hará un cultivo de las bolsas periodontales y de muestras de sangre (en el caso de bacteriemia). Empíricamente, se pueden pautar antibióticos para bacterias anaeróbicas como el metronidazol. Hay que tener en cuenta que el periodonto puede ser origen de infecciones fúngicas e infecciones virales reactivadas (Raber-Durlacher y cols. 2002).
A nivel de complicaciones locales, el tratamiento de los cánceres de cabeza y cuello afecta a las estructuras orales. Los síntomas agudos incluyen: mucositis, trastornos de la deglución, xerostomía y disgeusia. Los efectos tardíos incluyen disfagia, dolor, xerostomía, sensibilidad de las mucosas, alteraciones del gusto, trismo, caries y pérdida de inserción periodontal (García-Chías y cols. 2019).
Además, la osteorradionecrosis (ORN) es una complicación bien conocida de la radioterapia en la cabeza y el cuello. La mala higiene bucal, el mal estado periodontal, el historial de consumo de alcohol y tabaco y la dosis de radiación son factores de riesgo significativos (Owosho y cols. 2017).
En pacientes medicados con bifosfonatos orales se ha constatado osteonecrosis de la mandíbula (ONM) con una frecuencia variable según los estudios después de procedimientos periodontales, siendo los de mayor riesgo la amputación de la raíz (OR = 6,64), la extracción de dientes (OR = 3,7), la movilidad dental grave (OR = 3,60) y la herida no cerrada
(OR = 2,51) (Hasegawa y cols. 2017).
Pacientes periodontales que sobreviven al cáncer, pero no están en tratamiento oncológico activo
Es la situación más frecuente. A su vez, aquí hay dos tipos bien diferenciados:
A. Paciente que por haber tenido un cáncer de cabeza y cuello ha sido tratado con radioterapia sobre la cavidad oral y las glándulas salivares. Estos pacientes requieren atención en varios aspectos:
De una parte, se han de prevenir las secuelas locales, fundamentalmente atrofia mucosa, caries acelerada, xerostomía, pérdida de inserción periodontal, problemas de oclusión dental, trismo y osteonecrosis mandibular.
Por otro lado, es necesario realizar una detección precoz de las recidivas oncológicas del tumor tratado, así como de la aparición de segundas neoplasias como consecuencia de los factores de riesgo que produjeron el tumor primario anterior, como el tabaco, el alcohol o el VPH.
B. Paciente que ha sido tratado de tumores que no son primarios de cabeza y cuello y, por tanto, sin irradiación directa de la cavidad oral y de las glándulas salivares.
En estos casos hay que valorar que el paciente haya recuperado adecuadamente y sin déficits notables su estado inmunológico y hematológico y que no tenga secuelas como neutropenia o trombopenia que puedan alterar la frecuencia de complicaciones infecciosas o sangrado. Asimismo, es muy importante valorar la probabilidad de osteonecrosis mandibular por la medicación o factores de riesgo relacionados.
En general, el tratamiento periodontal en pacientes oncológicos puede realizarse sin problemas; las únicas limitaciones son las derivadas del tratamiento del proceso neoplásico, una vez normalizados los valores hematológicos y controlados los fármacos crónicos. Las visitas de mantenimiento se deben individualizar, variando entre 3 y 6 meses, siempre en contacto con el oncólogo.
CONCLUSIONES
EL CÁNCER ESTÁ MUY PRESENTE EN NUESTRA SOCIEDAD y por tanto en las
consultas dentales. Es necesario adquirir unas nociones básicas de oncología para tratar a muchos pacientes en diferentes etapas de su proceso oncológico, conociendo las posibles complicaciones derivadas de la enfermedad, de los tratamientos aplicados, o de nuestras posibles maniobras terapéuticas si no se está en constante contacto con los oncólogos.
Además, con el tiempo se han ido asociando la periodontitis avanzada y la pérdida dentaria notable con algunos tipos de cáncer, como ya se ha comentado, aunque no siempre por mecanismos aclarados. Sin embargo, parece que la actividad de un microbioma oral patogénico, la inflamación crónica de bajo grado y la inmunosupresión podrían influir en el desarrollo de algunos tipos de tumores, como los de la cavidad orofaríngea, tracto digestivo superior o páncreas. De otros tipos de tumores hay poca evidencia científica que permita la sospecha de una asociación entre estos dos tipos de enfermedades tan prevalentes (periodontitis y cáncer), entre otras cosas por limitaciones a la hora de establecer niveles de evidencia por factores como el problema del tabaco, o por problemas al diagnosticar la periodontitis por medios utilizados como la autoevaluación o el uso de medidas indirectas como la pérdida dentaria.
IMPLICACIONES PRÁCTICAS
Para los dentistas
Los pacientes con cáncer son un reto para el equipo odontológico, debido a su elevada prevalencia, la gravedad de los tipos, estadios y momento terapéutico de los tumores, así como por las complicaciones orales directas o provocadas por el tratamiento oncológico, y también por el odontológico en determinadas situaciones. De ahí la importancia de la prevención de este tipo de situaciones, siendo mandatorio el contacto continuado con los oncólogos. Debe motivarse al paciente en la consecución de unos hábitos de higiene bucodental adecuados de forma constante. Finalmente, el equipo dental es responsable directo de la detección precoz de los tumores orofaríngeos, así como de la educación de todos los pacientes sobre los factores de riesgo más relevantes para estos tumores y otras enfermedades generales, sobre todo el tabaco y el alcohol.
Para los oncólogos
El asesoramiento y colaboración con los dentistas ante los casos de cáncer debe formar parte del plan preventivo y terapéutico global del paciente. La información sobre el tipo de tumor, parámetros del mismo, indicaciones terapéuticas y su momento previsto de comienzo, así como sobre las posibles complicaciones esperables y su influencia en la consulta dental, indican la necesidad creciente de colaborar ambos profesionales por las ventajas evidentes para la situación bucodental y general del paciente. Existen grupos de oncólogos que incluyen la revisión odontológica y el control de la higiene bucodental en el “plan de acogida” al paciente recién diagnosticado de un tumor; es una excelente iniciativa que puede mejorar notablemente la situación general del enfermo de cáncer.
Para la población general
Concienciar al paciente y a la sociedad de la importancia de la higiene bucodental de forma preventiva y las revisiones regulares en el dentista antes de que se presenten enfermedades como el cáncer es mandatorio. Una boca bien cuidada garantiza menos complicaciones durante el tratamiento oncológico, algunas de las cuales pueden condicionar la interrupción temporal del mismo, aparte de generar complicaciones clínicas importantes a nivel oral y posteriormente general. El cáncer y su tratamiento disminuyen notablemente las defensas del paciente, favoreciendo la colonización o crecimiento de bacterias, virus y hongos en la cavidad oral, que muchas veces exigen tratamientos complejos y pueden poner en peligro la vida del paciente. Por eso es tan importante la comunicación oncólogo-dentista en todas las fases del tratamiento.
RELEVANCIA CLÍNICA
LA PREVENCIÓN DEL CÁNCER es de una gran responsabilidad en la consulta dental, comenzando sin duda por lo relacionado con el cáncer oral. Hay que tratar de modificar los hábitos de vida del paciente, intentando eliminar factores de riesgo tan importantes como el tabaco y/o el alcohol para tantos tipos de tumores. Una vez instaurada la enfermedad, es necesario adquirir unos conocimientos mínimos sobre su evolución y pronóstico, además del antes, durante y después del tratamiento oncológico, sobre todo en lo relacionado con la prevención y complicaciones orales derivadas del propio tumor o de su tratamiento. En este sentido, la comunicación oncólogo-dentista-paciente es absolutamente fundamental.
IMPLICACIONES PARA LA INVESTIGACIÓN
EL CAMPO POR RECORRER EN LA INVESTIGACIÓN sobre el cáncer es enorme, siendo muy relevante el estudio de los factores de riesgo de los distintos tipos
de tumores. La periodontitis forma parte del riesgo asociado para determinados cánceres, pero, en la mayoría de los casos, la evidencia es epidemiológica o biológica y ciertamente limitada para muchos tipos de tumores, por lo que el futuro está muy abierto a si existen más asociaciones periodontitis-cáncer, si estas tienen una
evidencia científica plausible, si la existente se puede incrementar y si la prevención y el tratamiento de la periodontitis pueden influir de alguna manera en la evolución de estas enfermedades tan graves para el ser humano.
REFERENCIAS BIBLIOGRÁFICAS
Abed H, Burke M, Scambler S, Scott SE. (2020) Denture use and osteoradionecrosis following radiotherapy for head and neck cancer: A systematic review. Gerodontology 37, 102-109.
Abnet CC, Kamangar F, Dawsey SM, Stolzenberg-Solomon RZ, Albanes D, Pietinen P, Virtamo J, Taylor PR. (2005) Tooth loss is associated with increased risk of gastric non-cardia adenocarcinoma in a cohort of Finnish smokers. Scandinavian Journal of Gastroenterology 40, 681-687.
Abnet CC, Kamangar F, Islami F, Nasrollahzadeh D, Brennan P, Aghcheli K, Merat S, Pourshams A, Marjani HA, Ebadati A, Sotoudeh M, Boffetta P, Malekzadeh R, Dawsey SM. (2008) Tooth loss and lack of regular oral hygiene are associated with higher risk of esophageal squamous cell carcinoma. Cancer Epidemiology, Biomarkers & Prevention 17, 3062-3068.
Ahn J, Segers S, Hayes RB. (2012) Periodontal disease, Porphyromonas gingivalis serum antibody levels and orodigestive cancer mortality. Carcinogenesis 33, 1055-
1058.
Amodini Rajakaruna G, Umeda M, Uchida K, Furukawa A, Yuan B, Suzuki Y, Noriko E, Izumi Y, Eishi Y. (2012) Possible translocation of periodontal pathogens into the lymph nodes draining the oral cavity. Journal of Microbiology (Seoul, Korea) 50, 827-836.
Anil S, Varma SV, Preethanath RS, Anand PS, Al Farraj, Aldosari A. (2012) The emerging concepts on the impact of periodontitis on systemic health. En: Manakil J, editores. Periodontal Diseases – A Clinician‘s Guide. IntechOpen, pág. 131-164.
Ansai T, Takata Y, Yoshida A, Soh I, Awano S, Hamasaki T, Sogame A, Shimada N. (2013) Association between tooth loss and orodigestive cancer mortality in an 80-year-old community-dwelling Japanese population: A 12-year prospective study. BMC Public Health 13, artículo 814.
Arora M, Weuve J, Fall K, Pedersen NL, Mucci LA. (2010) An exploration of shared genetic risk factors between periodontal disease and cancers: A prospective co-twin study. American Journal of Epidemiology 171, 253-259.
Baima G, Minoli M, Michaud DS, Aimetti M, Sanz M, Loos BG, Romandini M. (2024). Periodontitis and risk of cancer: Mechanistic evidence. Periodontology 2000 96, 83-94.
Balkwill F, Mantovani A. (2001) Inflammation and cancer: back to Virchow? Lancet 357, 539-545.
Bartlett JG, Gorbach SL, Finegold SM. (1974) The bacteriology of aspiration pneumonia. The American Journal of Medicine 56, 202-207.
Beech N, Robinson S, Porceddu S, Batstone M. (2014) Dental management of patients irradiated for head and neck cancer. Australian Dental Journal 59, 20-28.
Benites Condezo AF, Araujo RZ, Koga DH, Curi MM, Cardoso CL. (2021) Hyperbaric oxygen therapy for the placement of dental implants in irradiated patients: Systematic review and meta-analysis. The British Journal of Oral & Maxillofacial Surgery 59, 625-632.
Abnet CC, Qiao YL, Mark SD, Dong ZW, Taylor PR, Dawsey SM. (2001) Prospective study of tooth loss and incident esophageal and gastric cancers in China. Cancer Causes Control 12, 847-854.
Brennan MT, Woo SB, Lockhart PB. (2008) Dental treatment planning and management in the patient who has cancer. Dental Clinics of North America 52, 19-37.
Brook I, de Leyva F. (1994) Microbiology of tonsillar surfaces in infectious mononucleosis. Archives of Pediatrics & Adolescent Medicine 148, 171-1733.
Bundgaard T, Wildt J, Frydenberg M, Elbrond O, Nielsen JE. (1995) Case-control study of squamous cell cancer of the oral cavity in Denmark. Cancer Causes & Control 6, 57-67.
International Agency for Research on Cancer, World Health Organization. Cancer incidence in five continents. https://ci5.iarc.fr/Default.aspx
Carasol M, Llodra JC, Fernández-Meseguer A, Bravo M, García-Margallo MT, Calvo-Bonacho E, Sanz M, Herrera
D. (2016) Periodontal conditions among employed adults in Spain. Journal of Clinical Periodontology 43, 548-556.
Carrion J, Scisci E, Miles B, Sabino GJ, Zeituni AE, Gu Y, Bear A, Genco CA, Brown DL, Cutler CW. (2012) Microbial carriage state of peripheral blood dendritic cells (DCs) in chronic periodontitis influences DC differentiation, atherogenic potential. Journal of Immunology 189, 3178-3187.
Carvalho CG, Medeiros-Filho JB, Ferreira MC. (2018) Guide for health professionals addressing oral care for individuals in oncological treatment based on scientific evidence. Supportive Care in Cancer 26, 2651-2561.
Castellarin M, Warren RL, Freeman JD, et al.(2012) Fusobacterium nucleatum infection is prevalent in human colorectal carcinoma. Genome Research 22, 299-306.
Chang JS, Tsai C-R, Chen L-T, Shan Y-S. (2016) Investigating the association between periodontal disease and risk of pancreatic cancer. Pancreas 45, 134-141.
Chauncey HH, Muench ME, Kapur KK, Wayler AH. (1984) The effect of the loss of teeth on diet and nutrition. International Dental Journal 34, 98-104.
Chen H, Nie S, Zhu Y, Lu M. (2015) Teeth loss, teeth brushing and esophageal carcinoma: A systematic review and meta-analysis. Scientific Reports 5, artículo 15203.
Chen QL, Zeng XT, Luo ZX, Duan XL, Qin J, Leng WD. (2016) Tooth loss is associated with increased risk of esophageal cancer: Evidence from a meta-analysis with dose-response analysis. Scientific Reports 6, artículo 18900.
Chrcanovic BR, Albrektsson T, Wennerberg A. (2016) Dental implants in irradiated versus nonirradiated patients: A meta-analysis. Head & Neck 8, 448-481.
Chung SD, Tsai MC, Huang CC, Kao LT, Chen CH. (2016) A population- based study on the associations between chronic periodontitis and the risk of cancer. International Journal of Clinical Oncology 21, 219-223.
GBD 2019 Cancer Risk Factors Collaborators. (2022) The global burden of cancer attributable to risk factors, 2010-19: A systematic analysis for the Global Burden of Disease Study 2019. Lancet 400, 563-591.
Coussens LM, Werb Z. (2002) Inflammation and cancer. Nature 420, 860-867.
Cutler CW, Arnold RR, Schenkein HA. (1993) Inhibition of C3 and IgG proteolysis enhances phagocytosis of Porphyromonas gingivalis. Journal of Immunology 151, 7016-7029.
De Angelis R, Sant M, Coleman MP, Francisci S, Baili P, Pierannunzio D, Trama A, Visser O, Brenner H, Ardanaz E, Bielska-Lasota M, Engholm G, Nennecke A, Siesling S, Berrino F, Capocaccia R, EUROCARE-5 Working Group. (2014) EUROCARE-5 Working Group. Cancer survival in Europe 1999-2007 by country and age: results of EUROCARE-5-a population-based study. The Lancet. Oncology 15, 23-34.
Decker AM, Taichman LS, D’Silva NJ, Taichman RS. (2018) Periodontal treatment in cancer patients: An interdisciplinary approach. Current Oral Health Reports 5, 7-12.
Dharmani P, Strauss J, Ambrose C, Allen-Vercoe E, Chadee
K. (2011) Fusobacterium nucleatum infection of colonic cells stimulates MUC2 mucin and tumor necrosis factor alpha. Infection and Immunity 79, 2597-2607.
Divaris K, Olshan AF, Smith J, Bell ME, Weissler MC, Funkhouser WK, Bradshaw PT. (2010) Oral health and risk for head and neck squamous cell carcinoma: The Carolina Head and Neck Cancer Study. Cancer Causes Control 21, 567-575.
Dye BA, Wang R, Lashley R, Wei W, Abnet CC, Wang G, Dawsey SM, Cong W, Roth MJ, Li X, Qiao Y. (2007) Using NHANES oral health examination protocols as part of an esophageal cancer screening study conducted in a high-risk region of China. BMC Oral Health 7, artículo 10.
Esmaillzadeh A, Kimiagar M, Mehrabi Y, Azadbakht L, Hu FB, Willett WC. (2007) Dietary patterns and markers of systemic inflammation among Iranian women. The Journal of Nutrition 137, 992-998.
EUROSTAT. Tobacco consumption statistics. https:// ec.europa.eu/eurostat/statistics-explained/index.php/ Tobacco_consumption_statistics Federico A, Morgillo F, Tuccillo C, Ciardiello F, Loguercio
C. (2007) Chronic inflammation and oxidative stress in human carcinogenesis. International Journal of Cancer 121, 2381-2386.
Gaetti-Jardim E, Jr., Marcelino SL, Feitosa AC, Romito GA, Avila-Campos MJ. (20099 Quantitative detection of periodontopathic bacteria in atherosclerotic plaques from coronary arteries. Journal of Medical Microbiology 58 Pt 12, 1568-1575.
Gao S, Li S, Ma Z, Liang S, Shan T, Zhang M, Zhu X, Zhang P, Liu G, Zhou F, Yuan X, Jia R, Potempa J, Scott DA, Lamont RJ, Wang H, Feng X. (2016) Presence of Porphyromonas gingivalis in esophagus and its association with the clinicopathological characteristics and survival in patients with esophageal cancer. Infectious Agents and Cancer 11, artículo 3.
García-Chías B, Figuero E, Castelo-Fernández B, Cebrián- Carretero JL, Cerero-Lapiedra R. (2019) Prevalence of oral side effects of chemotherapy and its relationship with periodontal risk: A cross-sectional study. Supportive Care in Cancer 27, 3479-3490.
García-Gozalbo B, Cabañas-Alite L. (2021) A narrative review about nutritional management and prevention of oral mucositis in haematology and oncology cancer patients undergoing antineoplastic treatments. Nutrients 13, artículo 4075.
Garrote LF, Herrero R, Reyes RM, Vaccarella S, Anta JL, Ferbeye L, Muñoz N, Franceschi S. (2001) Risk factors for cancer of the oral cavity and oro-pharynx in Cuba. British Journal of Cancer 85, 46-54.
Genco RJ, Borgnakke WS. (2013) Risk factors for periodontal disease. Periodontology 2000 62, 59-94.
Goldstein EJ, Kirby BD, Finegold SM. (1979) Isolation of Eikenella corrodens from pulmonary infections. The American Review of Respiratory Disease 119, 55-58.
Graham S, Dayal H, Rohrer T, et al. (1977) Dentition, diet, tobacco, and alcohol in the epidemiology of oral cancer. Journal of the National Cancer Institute 59, 1611-1618.
Guha N, Boffetta P, Wunsch Filho V, Eluf Neto J, Shangina O, Zaridze D, Curado MP, Koifman S, Matos E, Menezes A, Szeszenia-Dabrowska N, Fernandez L, Mates D, Daudt AW, Lissowska J, Dikshit R, Brennan P. (2007) Oral health and risk of squamous cell carcinoma of the head and neck and esophagus: Results of two multicentric case-control studies. American Journal of Epidemiology 166, 1159-1173.
Hanahan D. (2022) Hallmarks of Cancer: new dimensions.
Cancer Discovery 12, 31-46.
Haraszthy VI, Zambon JJ, Trevisan M, Zeid M, Genco RJ. (2000) Identification of periodontal pathogens in atheromatous plaques. The Journal of Periodontology 71, 1554-1560.
Hasegawa T, Kawakita A, Ueda N, Funahara R, Tachibana A, Kobayashi M, Kondou E, Takeda D, Kojima Y, Sato S, Yanamoto S, Komatsubara H, Umeda M, Kirita T, Kurita H, Shibuya Y, Komori T. (2017) A multicenter retrospective study of the risk factors associated with medication-related osteonecrosis of the jaw after tooth extraction in patients receiving oral bisphosphonate therapy: can primary wound closure and a drug holiday really prevent MRONJ? Osteoporosis International 28, 2465-2473.
Heikkila P, But A, Sorsa T, Haukka J. (2018) Periodontitis and cancer mortality: Register-based cohort study of 68,273 adults in 10-year follow-up. International Journal of Cancer 142, 2244-2253.
Hiraki A, Matsuo K, Suzuki T, Kawase T, Tajima K. (2008) Teeth loss and risk of cancer at 14 common sites in Japanese. Cancer Epidemiology, Biomarkers & Prevention 17, 1222-1227.
Hong CH, Hu S, Haverman T, Stokman M, Napeñas JJ, Bos- den Braber J, Gerber E, Geuke M, Vardas E, Waltimo T, Jensen SB, Saunders DP. (2018) A systematic review of dental disease management in cancer patients. Supportive Care in Cancer 26, 155-174.
Huang J, Roosaar A, Axéll T, Ye W. (2016) A prospective cohort study on poor oral hygiene and pancreatic cancer risk. International Journal of Cancer 138, 340- 347.
Hujoel PP, Drangsholt M, Spiekerman C, Weiss NS. (2003) An exploration of the periodontitis-cancer association. Annals of Epidemiology 13, 312-316.
Hwang I-M, Sun L-M, Lin C-L, Lee C-F, Kao C-H. (2014)
Periodontal disease with treatment reduces subsequent cancer risks. QJM: Monthly Journal of the Association of Physicians 107, 805-812.
Instituto Nacional de Estadística (INE). Estadística de defunciones según la causa de muerte 2023. https:// www.ine.es/dyngs/Prensa/pEDCM2023.htm
Kauppila JH, Mattila AE, Karttunen TJ, Salo T. (2013) Toll- like receptor 5 (TLR5) expression is a novel predictive marker for recurrence and survival in squamous cell carcinoma of the tongue. British Journal of Cancer 108, 638-643.
Kauppila JH, Mattila AE, Karttunen TJ, Salo T. (2013) Toll- like receptor 5 and the emerging role of bacteria in carcinogenesis. Oncoimmunology 2, artículo e23620.
Kostic AD, Chun E, Robertson L, Glickman JN, Gallini CA, Michaud M, Clancy TE, Chung DC, Lochhead P, Hold GL, El-Omar EM, Brenner D, Fuchs CS, Meyerson M, Garrett WS. (2013) Fusobacterium nucleatum potentiates intestinal tumorigenesis and modulates the tumor-immune microenvironment. Cell Host & Microbe 14, 207-215.
Kostic AD, Gevers D, Pedamallu CS, Michaud M, Duke F, Earl AM, Ojesina AI, Jung J, Bass AJ, Tabernero J, Baselga J, Liu C, Shivdasani RA, Ogino S, Birren BW, Huttenhower C, Garrett WS, Meyerson M. (2012) Genomic analysis identifies association of Fusobacterium with colorectal carcinoma. Genome Research 22, 292-298.
Kurita H, Umeda M, Ueno T, Uzawa N, Shibuya Y, Nakamura N, Nagatsuka H, Hayashi T, Mizoguchi I, Tomihara K, Ikegami Y, Noguchi K, Takiguchi Y, Yamamoto N, Sakai
H. (2024) Management of odontogenic foci of infection (dental caries, periodontal disease and odontogenic infections) in the oral functional management of patients receiving cancer treatments: Guidelines based on a systematic review. Oral Science International 21, 161-180.
Lalla E, Lamster IB, Stern DM, Schmidt AM. (2001) Receptor for advanced glycation end products, inflammation, and accelerated periodontal disease in diabetes: mechanisms and insights into therapeutic modalities. Annals of Periodontology D6, 113-118.
Le Moal G, Juhel L, Grollier G, Godet C, Azais I, Roblot F. (2005) Vertebral osteomyelitis due to Fusobacterium species: Report of three cases and review of the literature. The Journal of Infection 51, e5-e9.
Lissowska J, Pilarska A, Pilarski P, Samolczyk-Wanyura D, Piekarczyk J, Bardin-Mikolłajczak A, Zatonski W, Herrero R, Muñoz N, Franceschi S. (2003) Smoking, alcohol, diet, dentition and sexual practices in the epidemiology of oral cancer in Poland. European Journal of Cancer Prevention 12, 25-33.
Logsdon CD, Fuentes MK, Huang EH, Arumugam T. (2007) RAGE and RAGE ligands in cancer. Current Molecular Medicine 7, 777-789.
Loo WT, Jin L, Cheung MN, Wang M, Chow LW. (2010) Epigenetic change in E-cadherin and COX-2 to predict chronic periodontitis. Journal of Translational Medicine 8, artículo 110.
Lowenberg B, Downing JR, Burnett A. (1999) Acute myeloid leukemia. The New England Journal of Medicine 34, 1051-1062.
Maier H, Zoller J, Herrmann A, Kreiss M, Heller WD. (1993) Dental status and oral hygiene in patients with head and neck cancer. Otolaryngology Head and Neck Surgery 108, 655-661.
Maisonneuve P, Amar S, Lowenfels AB. (2017) Periodontal disease, edentulism, and pancreatic cancer: A meta- analysis. Annals of Oncology 28, 985-995.
Mantovani A, Allavena P, Sica A, Balkwill F. (2008) Cancer- related inflammation. Nature 454, 436-444.
Marshall JR, Graham S, Haughey BP, et al. (1992) Smoking, alcohol, dentition and diet in the epidemiology of oral cancer. European Journal of Cancer. Part B, Oral Oncology 28B, 9-15.
Massler CF, Jr. (2000) Preventing and treating the oral complications of cancer therapy. General Dentistry 48, 652-655.
Mazul AL, Shivappa N. (2018) Proinflammatory diet is associated with increased risk of squamous cell head and neck cancer. The International Journal of Cancer 143, 1604-1610.
Mege JL, Mehraj V, Capo C. (2011) Macrophage polarization and bacterial infections. Current Opinion in Infectious Diseases 24, 230-234.
Meyer MS, Joshipura K, Giovannucci E, Michaud DS. (2008) A review of the relationship between tooth loss, periodontal disease, and cancer. Cancer Causes & Control 19, 895-907.
Michaud DS, Joshipura K, Giovannucci E, Fuchs CS. (2007) A prospective study of periodontal disease and pancreatic cancer in US male health professionals. Journal of the National Cancer Institute 99, 171-175.
Michaud DS, Liu Y, Meyer M, Giovannucci E, Joshipura K. (2008) Periodontal disease, tooth loss, and cancer risk in male health professionals: A prospective cohort study. The Lancet Oncology 9, 550-558.
Michaud DS, Kelsey KT, Papathanasiou E, Genco CA, Giovannucci E. (2016) Periodontal disease and risk of all cancers among male never smokers: An updated analysis of the health professionals follow-up study. Annals of Oncology 27, 941-947.
Michaud DS, Fu Z, Shi J, Chung M. (2017) Periodontal disease, tooth loss, and cancer risk. Epidemiologic Reviews 39, 49-58.
Michaud DS, Lu J, Peacock-Villada AY, Barber JR, Joshu CE, Prizment AE, Beck JD, Offenbacher S, Platz EA. (2018) Periodontal disease assessed using clinical dental measurements and cancer risk in the ARIC Study. Journal of the National Cancer Institute 110, 843-854.
Moergel M, Kämmerer P, Kasaj A, Armouti E, Alshihri A, Weyer V, Al-Nawas B. (2013) Chronic periodontitis and its possible association with oral squamous cell carcinoma-A retrospective case control study. Head & Face Medicine 9, artículo 39.
Sociedad Española de Onconlogía Médica, Sociedad Española de Enfermería Oncológica, Sociedad Española de Ortodoncia y Ortopedia Dentofacial. (2022) Multidisciplinary consensus on oral care in cancer patients. https://agsjerez.es/wp-content/ uploads/2024/11/A.F.CONSENSO_ORTODONCIA.
Namazi N, Larijani B, Azadbakht L. (2018) Association between the dietary inflammatory index and the incidence of cancer: A systematic review and meta- analysis of prospective studies. Public Health 164, 148- 156.
Narikiyo M, Tanabe C, Yamada Y, Igaki H, Tachimori Y, Kato H, Muto M, Montesano R, Sakamoto H, Nakajima Y, Sasaki H. (2004) Frequent and preferential infection of Treponema denticola, Streptococcus mitis, and Streptococcus anginosus in esophageal cancers. Cancer Science 95, 569-574.
National Cancer Institute. Oral Complications of Chemotherapy and Head/Neck Radiation (PDQ®) Health Professional Version. https://www.cancer.gov/ about-cancer/treatment/side-effects/mouth-throat/oral- complications-hp-pdq
Nwizu NN, Marshall JR, Moysich K, Genco RJ, Hovey KM, Mai X, LaMonte MJ, Freudenheim JL, Wactawski- Wende J. (2017) Periodontal disease and incident cancer risk among postmenopausal women: Results from the women‘s health initiative observational cohort. Cancer Epidemiology, Biomarkers & Prevention 26, 1255-1265.
Owosho AA, Tsai CJ, Lee RS, Freymiller H, Kadempour A, Varthis S, Sax AZ, Rosen EB, Yom SK, Randazzo J, Drill E, Riedel E, Patel S, Lee NY, Huryn JM, Estilo CL. (2017) The prevalence and risk factors associated with osteoradionecrosis of the jaw in oral and oropharyngeal cancer patients treated with intensity-modulated radiation therapy (IMRT): The Memorial Sloan Kettering Cancer Center experience. Oral Oncology 64, 44-51.
Padilla C, Lobos O, Hubert E, González C, Matus S, Pereira M, Hasbun S, Descouvieres C. (2006) Periodontal pathogens in atheromatous plaques isolated from patients with chronic periodontitis. Journal of Periodontal Research 41, 350-353.
Page RC. (1998) The pathobiology of periodontal diseases may affect systemic diseases: Inversion of a paradigm. Annals of periodontology 3, 108-120.
Peters BA, Wu J, Pei Z, Yang L, Purdue MP, Freedman ND, Jacobs EJ, Gapstur SM, Hayes RB, Ahn J. (2017) Oral microbiome composition reflects prospective risk for esophageal cancers. Cancer Research 77, 6777-6787.
Philipone EM, Peters SM. (2023) Ulcerative and inflammatory lesions of the oral mucosa. Oral and Maxillofacial Surgery Clinics of North America 35, 219-226.
Ministerio de Sanidad. (2024) Plan Integral de Prevención y Control del Tabaquismo 2024-2027. https://tinyurl. com/23b989la
Plummer M, de Martel C, Vignat J, Ferlay J, Bray F, Franceschi
S. (2016) Global burden of cancers attributable to infections in 2012: A synthetic analysis. The Lancet Global Health 4, e609-e616.
Pulendran B, Kumar P, Cutler CW, Mohamadzadeh M, Van Dyke T, Banchereau J. (2001) Lipopolysaccharides from distinct pathogens induce different classes of immune responses in vivo. Journal of Immunology 167, 5067- 5076.
Pushalkar S, Ji X, Li Y, Estilo C, Yegnanarayana R, Singh B, Li X, Saxena D. (2012) Comparison of oral microbiota in tumor and non-tumor tissues of patients with oral squamous cell carcinoma. BMC Microbiology 12, artículo 144.
Raber-Durlacher JE, Epstein JB, Raber J, van Dissel JT, van Winkelhoff A, Guiot HF, van der Velden U. (2002) Periodontal infection in cancer patients treated with high-dose chemotherapy. Supportive Care in Cancer 10, 466-473.
Rankin KV, Epstein J, Hubber MA, Peterson DE, Plemons JM, Redding SS, Sanfillippo NJ, Schubert MM, Sonis ST. (2009) Oral health in cancer therapy. Todays FDA 37, 39-45.
Recalde M, Pistillo A, Viallon V, Fontvieille E, Duarte- Salles T, Freisling H. (2023) Body mass index and incident cardiometabolic conditions in relation to obesity-related cancer risk: A population-based cohort study in Catalonia, Spain. Cancer Medicine 12, 20188-20200.
Red Española de Registros de Cáncer. https:// www. redecan.org
Rezende CP, Ramos MB, Daguila CH, Dedivitis RA, Rapoport A. (2008) Oral health changes in with oral and oropharyngeal cancer. Brazilian Journal of Otorhinolaryngology 74, 596-600.
Rubinstein MR, Wang X, Liu W, Hao Y, Cai G, Han YW. (2013) Fusobacterium nucleatum promotes colorectal carcinogenesis by modulating E-cadherin/beta-catenin signaling via its FadA adhesin. Cell Host & Microbe 14, 195-206.
Ruggiero SL, Dodson TB, Fantasia J, Goodday R, Aghaloo TA, Mehrotra B, O‘Ryan F; American Association of Oral and Maxillofacial Surgeons. (2014) American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw– 2014 update. Journal of Oral and Maxillofacial Surgery 72, artículo 193856.
Rumgay H, Shield K, Charvat H, Ferrari P, Sornpaisarn B, Obot I, Islami F, Lemmens VEP, Rehm J, Soerjomataram
I. (2021) Global burden of cancer in 2020 attributable to alcohol consumption: A population-based study. The Lancet Oncology 22, 1071-1080.
Salazar CR, Sun J, Li Y, Francois F, Corby P, Pérez-Pérez G, Dasanayake A, Pei Z, Chen Y. (2013) Association between selected oral pathogens and gastric precancerous lesions. PLoS One 8, artículo e51604.
Sasaki H, Ishizuka T, Muto M, Nezu M, Nakanishi Y, Inagaki Y, Watanabe H, Terada M. (1998) Presence of Streptococcus anginosus DNA in esophageal cancer, dysplasia of esophagus, and gastric cancer. Cancer Research 58, 2991-2995.
Sasaki M, Yamaura C, Ohara-Nemoto Y, Tajika S, Kodama Y, Ohya T, Harada R, Kimura S. (2005) Streptococcus anginosus infection in oral cancer and its infection route. Oral Diseases 11, 151-156.
Shakeri R, Malekzadeh R, Etemadi A, Nasrollahzadeh D, Ardekani BA, Khoshnia M, Islami F, Pourshams A, Pawilta M, Boffetta P, Dawsey SM, Kamangar F, Abnet
CC. (2013) Association of tooth loss and oral hygiene with risk of gastric adenocarcinoma. Cancer Prevention Research 6, 477-482.
Shivappa N, Prizment AE, Blair CK, Jacobs DR, Jr., Steck SE, Hebert JR. (2014) Dietary inflammatory index and risk of colorectal cancer in the Iowa Women‘s Health Study. Cancer Epidemiology, Biomarkers & Prevention 23, 2383-2392.
Stolzenberg-Solomon RZ, Dodd KW, Blaser MJ, Virtamo J, Taylor PR, Albanes D. (2003) Tooth loss, pancreatic cancer, and Helicobacter pylori. The American Journal of Clinical Nutrition 78, 176-181.
Strauss J, Kaplan GG, Beck PL, Rioux K, Panaccione R, Devinney R, Lynch T, Allen-Vercoe E. (2011) Invasive potential of gut mucosa-derived Fusobacterium nucleatum positively correlates with IBD status of the host. Inflammatory Bowel Diseases 17, 1971-1978.
Subapriya R, Thangavelu A, Mathavan B, Ramachandran CR, Nagini S. (2007) Assessment of risk factors for oral squamous cell carcinoma in Chidambaram, Southern India: A case-control study. European Journal of Cancer Prevention 16, 251-256.
Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, Bray F. (2021) Global Cancer Statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: A Cancer Journal for Clinicians 71, 2029-2049.
Swidsinski A, Dorffel Y, Loening-Baucke V, Theissig F, Rückert JC, Ismail M, Rau WA, Gaschler D, Weizenegger M, Kühn S, Schilling J, Dörffel WV. (2011) Acute appendicitis is characterised by local invasion with Fusobacterium nucleatum/necrophorum. Gut 60, 34-40.
Talamini R, Vaccarella S, Barbone F, Tavani A, La Vecchia C, Herrero R, Muñoz N, S Franceschi S.(2000) Oral hygiene, dentition, sexual habits and risk of oral cancer. British Journal of Cancer 83, 1238-1242.
Tezal M, Grossi SG, Genco RJ. (2005) Is periodontitis associated with oral neoplasms? Journal of Periodontology 76, 406-410.
Tezal M, Sullivan MA, Reid ME, Marshall JR, Hyland A, Loree T, Lillis C, Hauck L, Wactawski-Wende J, Scannapieco FA. (2007) Chronic periodontitis and the risk of tongue cancer. Archives of Otolaryngology–Head & Neck Surgery 133, 450-454.
Tezal M, Sullivan Nasca M, Stoler DL, Melendy T, Hyland A, Smaldino PJ, Rigual NR, Loree TR. (2009) Chronic periodontitis-human papillomavirus synergy in base of tongue cancers. Archives of Otolaryngology–Head & Neck Surgery 135, 391-396.
Truant AL, Menge S, Milliorn K, Lairscey R, Kelly MT. (1983) Fusobacterium nucleatum pericarditis. Journal of Clinical Microbiology 17, 349-351.
Velly AM, Franco EL, Schlecht N, Pintos J, Kowalski LP, Oliveira BV, Curado MP. (1998) Relationship between dental factors and risk of upper aerodigestive tract cancer. Oral Oncology 34, 284-291.
Verdecchia A, Micheli A, Colonna M, Moreno V, Izarzugaza MI, Paci E, EUROPREVAL Working Group. (2002) A comparative analysis of cancer prevalence in cancer registry areas of France, Italy and Spain. Annals of Oncology 13, 1128-1139.
Vozza I, Caldarazzo V, Polimeni A, Ottolenghi L. (2015) Periodontal disease and cancer patients undergoing chemotherapy. International Dental Journal 65, 45-48.
Walls AW, Steele JG, Sheiham A, Marcenes W, Moynihan PJ. (2000) Oral health and nutrition in older people. Journal of Public Health Dentistry 60, 304-307.
Winn DM, Blot WJ, McLaughlin JK, Austin DF, Greenberg RS, Preston-Martin S, Schoenberg JB, Fraumeni JF Jr. (1991) Mouthwash use and oral conditions in the risk of oral and pharyngeal cancer. Cancer Research 51, 3044-3047.
World Cancer Research Fund, American Institute for Cancer Research. (2007) Food, Nutrition, Physical Activity, and the Prevention of Cancer: A Global Perspective. https:// tinyurl.com/26feqrvg
Yin XH, Wang YD, Luo H, Zhao K, Huang GL, Luo SY, Peng JX, Song JK. (2016) Association between tooth loss and gastric cancer: A meta-analysis of observational studies. PLoS One 11, artículo e0149653.
Yoneda M, Naka S, Nakano K, Wada K, Endo H, Mawatari H, Imajo K, Nomura R, Hokamura K, Ono M, Murata S, Tohnai I, Sumida Y, Shima T, Kuboniwa M, Umemura K, Kamisaki Y, Amano A, Okanoue T, Ooshima T, Nakajima A. (2012) Involvement of a periodontal pathogen, Porphyromonas gingivalis on the pathogenesis of non-alcoholic fatty liver disease. BMC Gastroenterology 12, artículo 16.
Zeng XT, Deng AP, Li C, Xia LY, Niu YM, Leng WD. (2013) Periodontal disease and risk of head and neck cancer: A meta-analysis of observational studies. PLoS One 8, artículo e79017.
Zeng XT, Luo W, Huang W, Wang Q, Guo Y. (2013) Tooth Loss and head and neck cancer: A meta-analysis of observational studies. Plos One 8, artículo e79074.
Zheng TZ, Boyle P, Hu HF, Duan J, Jian PJ, Ma DQ, Shui LP, Niu SR, Scully C, MacMahon B. (1990) Dentition, oral hygiene, and risk of oral cancer: A case-control study in Beijing, People‘s Republic of China. Cancer Causes & Control 1, 235-241.

